
فيروس الإنفلونزا ولماذا لم نقضِ عليه حتى الآن؟
بقلم :عمر غانم
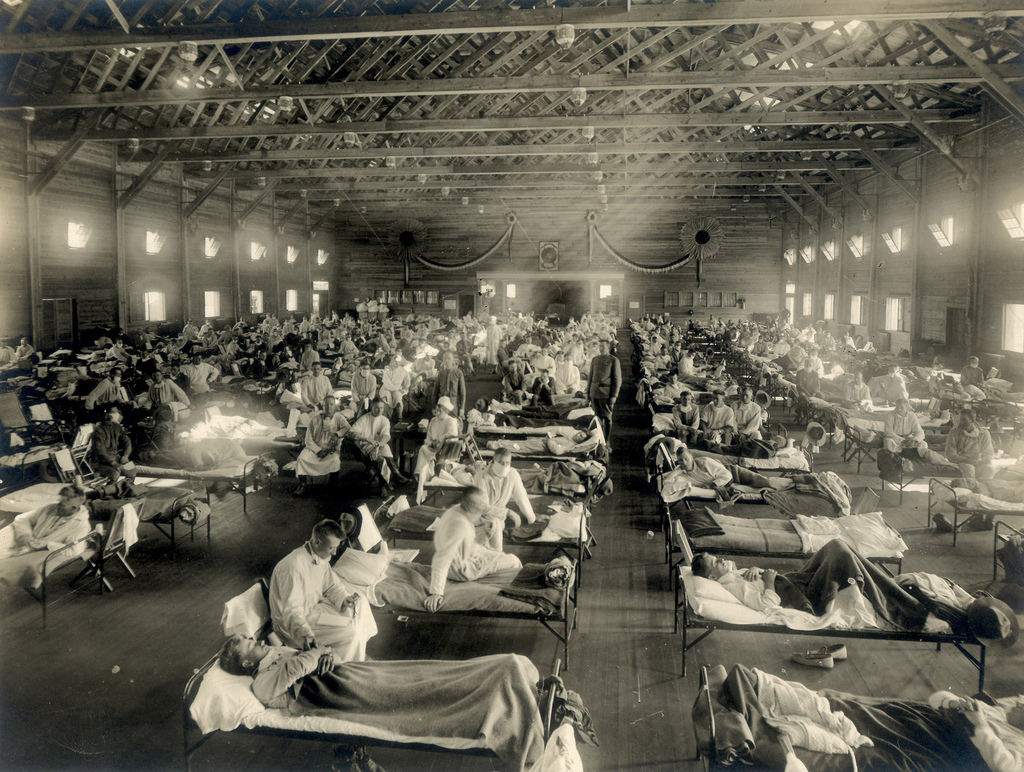
وباء عام 1918
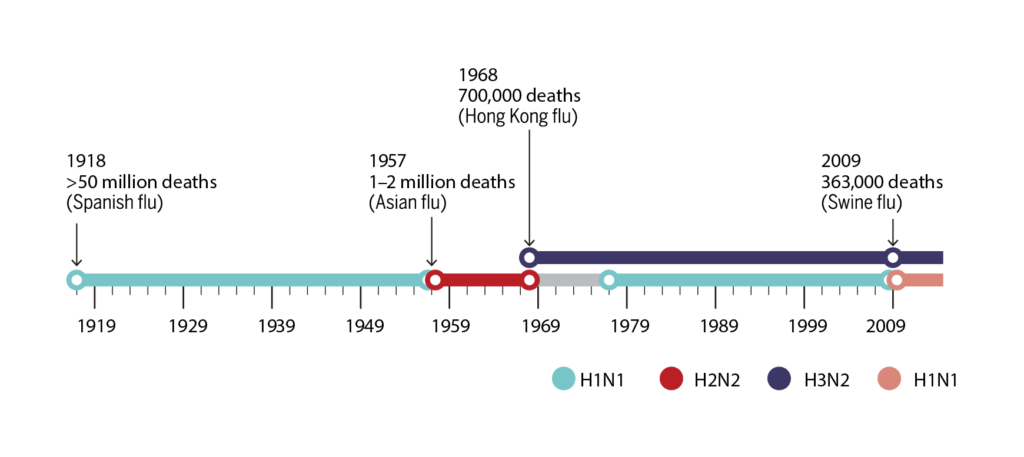
تاريخيًا خلّف فيروس الإنفلونزا الأسبانية عام 1918 حوالي 50 مليون قتيلٍ وكان ذلك لسوء الحظ متزامنًا مع الحرب العالمية الأولى التي ساعدت على انتشاره بالإضافة إلى عوامل أخرى -فلا تأتي المصائب فرادى على ما يبدو!-، وتتابعت أوبئة الإنفلونزا حتى كان آخرها عام 2009 فيما يُعرف بإنفلونزا الخنازير، لكنّ تتابع هذه الأوبئة لم يكن سيئًا تمامًا، فقد ألقى الضوء على حاجتنا إلى فهم فيروس الإنفلونزا بشكلٍ أعمق، ورُغم التقدم الكبير في علم البيولوجيا الجزيئية والفيروسات، إلا أن هناك بعض التحديات التي لم نجد لها حلاً حتى الآن.
فيروس الإنفلونزا
تُقسّم «اللجنة الدولية لتصنيف الفيروسات» (ICTV) فيروس الإنفلونزا إلى ثلاثة أنواع رئيسية هي: (A و Bو C) بناءً على عدة عوامل مثل المادة الوراثية والتركيب ونطاق العوائل التي يصيبها، ولهذه الأنواع الثلاث تركيبٌ متشابهٌ تقريبًا عدا بعض الاختلافات الطفيفة؛ فمن حيث العوائل التي تصيبها، يصيبُ النوع (A) نطاقًا واسعًا من العوائل مما يجعله الأكثر خطورة والأكثر عرضة للطفرات الوراثية،
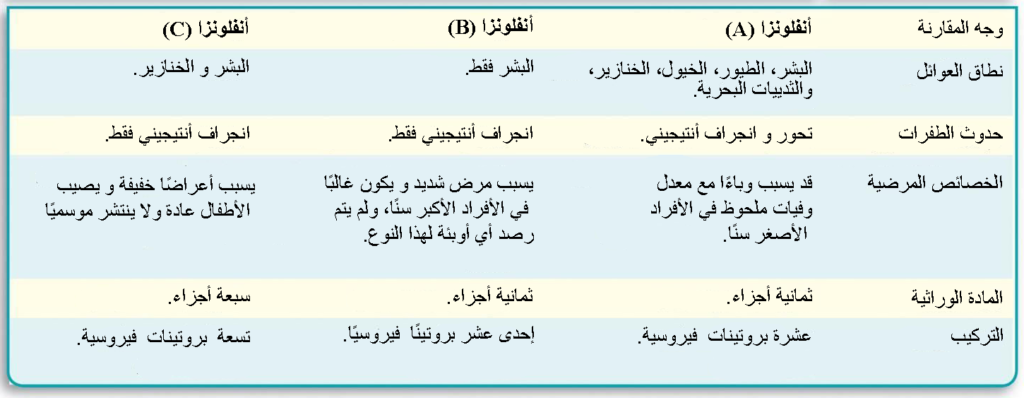
ولهذا سيكون مثالًا مناسبًا للحديث عن خصائص فيروس الإنفلونزا.
تركيب فيروس الإنفلونزا
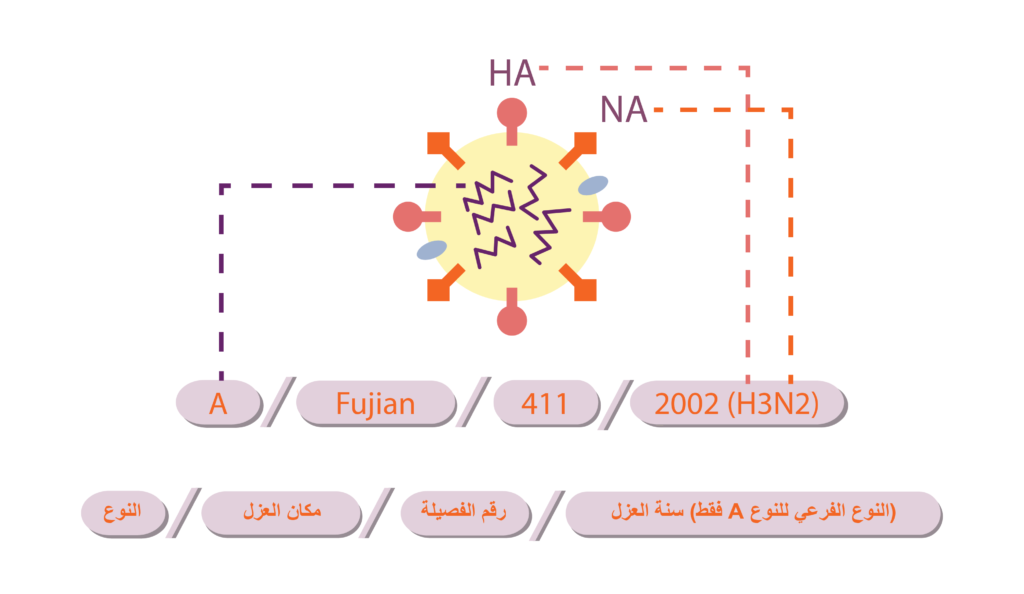
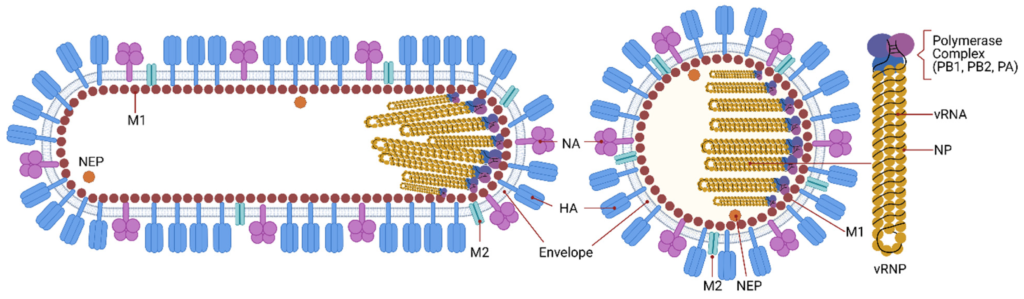
يتخذ فيروس الإنفلونزا شكلًا كرويًا أو خيطيًا، وتتكون المادة الوراثية له من «الحمض النووي الريبوزي مفرد الشريط» (ssRNA) وتنقسم إلى ثمانية أجزاء في النوعين (A وB) وسبعة في النوع (C). تلتف المادة الوراثية حلزونيًا بمساعدة مجموعة من «البروتينات النووية» (Nucleoproteins, NP)، حيث يحمل كل جزء منها معلومة وراثية لبناء بروتين واحد أو أكثر، فالنوع (A) مثلًا يحتوي على ثمانية أجزاء تحمل معلومات وراثية لعشرة بروتينات، ويوجد عند بداية كل جزء إنزيم بلمرة خاص يسمى «إنزيم بلمرة الحمض النووي الريبوزي المعتمد على الحمض النووي الريبوزي» (RNA-dependent RNA Polymerase, RdRp)، ويتخذ هذا الإنزيم الحمضَ النوويَّ الريبوزي قالبًا له لتكوين حمضٍ نووي ريبوزي جديد يتكون من ثلاث وحدات (PB1 و PB2و PA) لذلك يسمى كل جزء بـ «البروتين الحمضي النووي الريبوزي الفيروسي» (Ribonucleoprotein, vRNP). ويحاط فيروس الإنفلونزا من الخارج بغشاء دهني، ويبطنه من الداخل بروتين القالب (M1, Matrix Protein)، ويتخلل هذا الغشاء «بروتينات شوكية» (Spike Proteins) هي «الهيماجلوتينين» (Hemagglutinin, HA,H) الذي يساعد الفيروس على الارتباط بخلايا العائل ويوجد منه 16 نوعًا في النوع (A) من فيروس الإنفلونزا، و«النورامينيداز» (Neuraminidase, NA,N) الذي يعمل على تحرير الفيروس ليخرج من الخلية ويوجد منه 9 أنواع في النوع (A)، لذلك نجد أن تسمية فيروسات الإنفلونزا من النوع (A) تشتمل على رموز وأرقام تدل على نوع البروتينات الشوكية الموجودة في هذه الفيروسات مثل (H1N1 وH2N1 وH5N1.. إلخ)، كما توجد البروتينات (M2 وNS1 وNS2/NEP) التي تساعد الفيروس على التضاعف وتزيد من قدرته على إحداث المرض.

دورة تضاعف فيروس الإنفلونزا
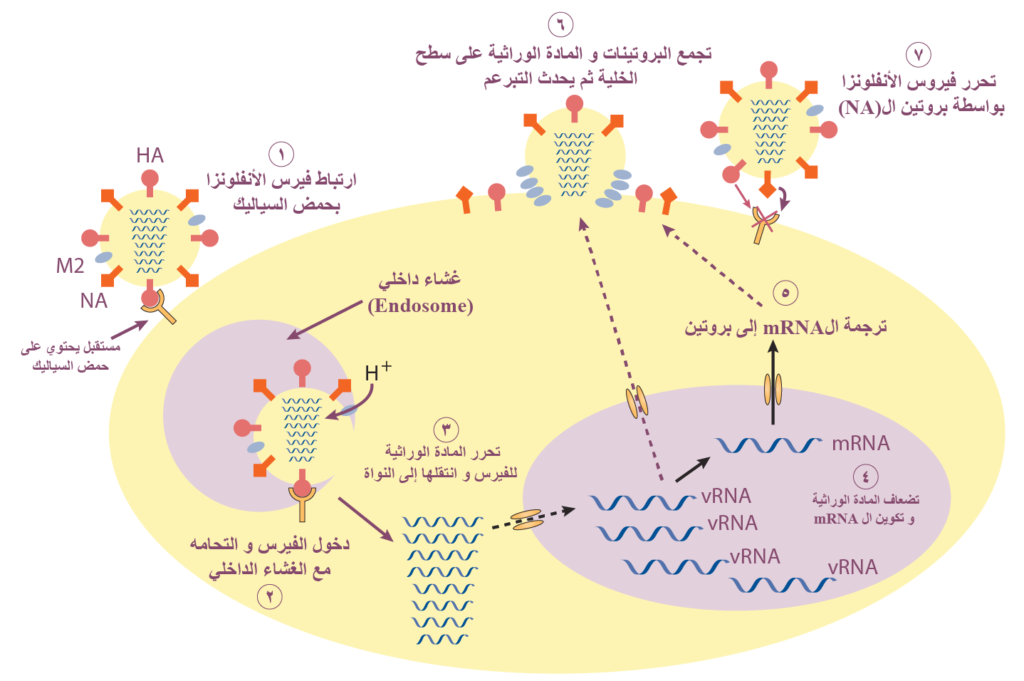
ينتشر فيروس الإنفلونزا في الهواء أو عن طريق لمس الأسطح الملوثة، فينتقل من خلال الأنف أو الفم إلى المجرى الهوائي ثم إلى الجهاز التنفسي وتمثل «الخلايا الطلائية» (Epithelial Cells) للجهاز التنفسي الهدف الأساسي لفيروس الإنفلونزا حيث يرتبط البروتين (HA) بحمض السياليك الموجود بكثرة على سطح الخلايا الطلائية، مما يؤدي إلى دخول الفيروس إليها محاطًا بـ «غشاء داخلي» (Endosome)، ثم يأتي دور البروتين (M2) الذي يعمل كمضخة لأيونات الهيدروجين، ويؤدي ذلك إلى تغيُّرٍ في تركيب البروتين (HA) فيلتحم غشاء الفيروس بالغشاء الداخلي وتتحرر مادته الوراثية ثم تنتقل إلى النواة لتبدأ في التضاعف، وهناك تُنتج جزيئات «الحمض النووي الريبوزي الرسول» (mRNA) الخاصة بالبروتينات الفيروسية لتتم ترجمتها في سيتوبلازم الخلية، ثم تنتقل إلى غشاء الخلية وتتجمع لتحيط ببعضها البعض فتنتج فيروسًا جديدًا في عملية يطلق عليها «التبرعم» (Budding).
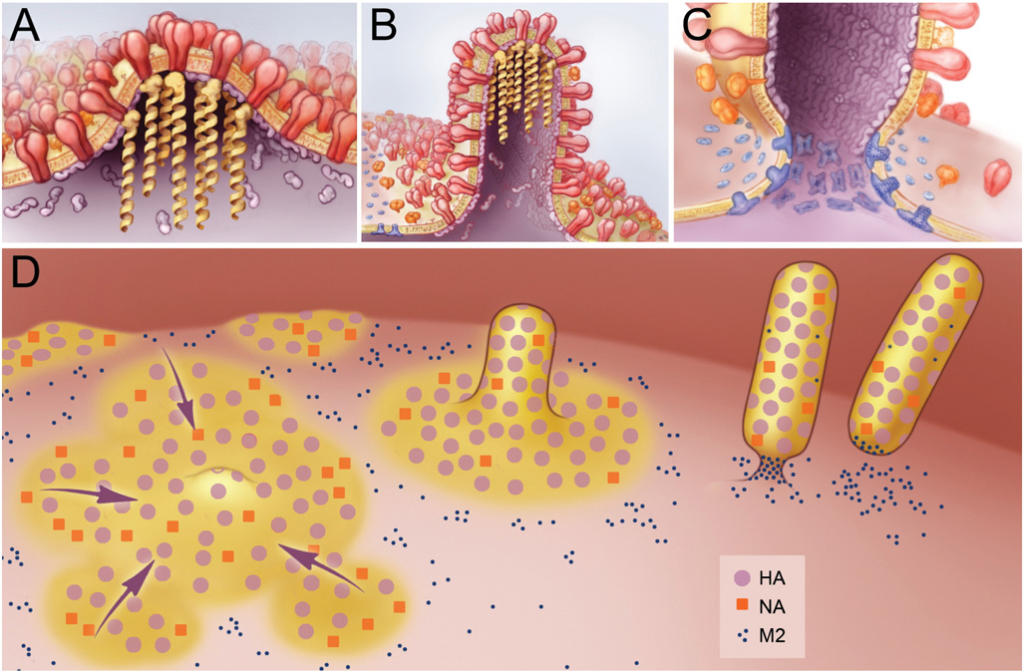
تلعب البروتينات (M1 وM2 وNA) دورًا أساسيًا في عملية التبرعم حيث يبطن بروتين (M1) غشاء الخلية من الداخل فتبدأ جزيئات (vRNP) بالتكدس ويمتد الفيروس المتبرعم للخارج مكونًا شكلًا كرويًا أو شريطيًا، ثم يتجمع بروتين (M2) عند بداية الفيروس المتبرعم ليعمل على التحام غشاء الفيروس، ويتحرر لإنتاج جزيء فيروسي جديد، ويعمل بروتين (NA) على منع ارتباط الفيروس بحمض السياليك مرة أخرى ليتمكن الفيروس من التحرر ومهاجمة خلية أخرى.
لماذا لم نجد حلًا نهائيًا لفيروس الإنفلونزا؟
لأن فيروس الإنفلونزا يحتوي على مادة وراثية من (RNA) ويفتقر إنزيم التضاعف الفيروسي (RdRp) إلى القدرة على تصحيح الأخطاء، ونظرًا لأن المادة الوراثية لفيروس الإنفلونزا مقسّمة إلى عدة أجزاء مستقلة، نجد معدل تغيّر فيروس الإنفلونزا كبيرًا، حيث يمكّنه من التحور وتخطي الدفاعات المناعية.
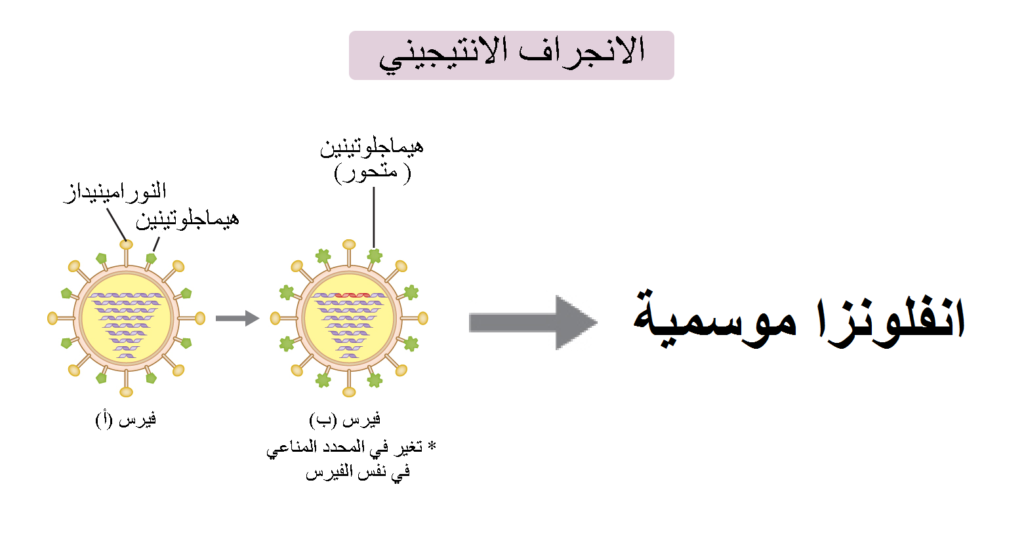
ينتج جهازنا المناعي الأجسام المضادة بصفة أساسية لمقاومة الفيروسات بالإضافة إلى آليات أخرى، حيث ترتبط الأجسام المضادة بتتابع معين من الأحماض الأمينية في البروتينات الشوكية (HA) و(NA) يسمى «المحدد المناعي» (Epitope) أو (Antigenic Determinant). ونظرًا لأن معدل التغير في الشفرة الوراثية للبروتينات الشوكية قد يكون الأكبر، فإن تركيب هذه المحددات في تغير مستمر، وأي تغير بسيط في الشفرة الوراثية لحمض أميني واحد في تركيب هذه المحددات المناعية يؤدي إلى عجز الأجسام المضادة في الارتباط بالفيروس مما يتسبب في حدوث العدوى مجددًا أكثر من مرة خلال العام الواحد، فتحدث الإنفلونزا الموسمية نتيجة لما يسمى بـ «الانجراف الأنتيجيني» (Antigenic Drift)، لذلك نحتاج إلى تحديث مستمر للقاحات الإنفلونزا لمواكبة هذه التغيرات.
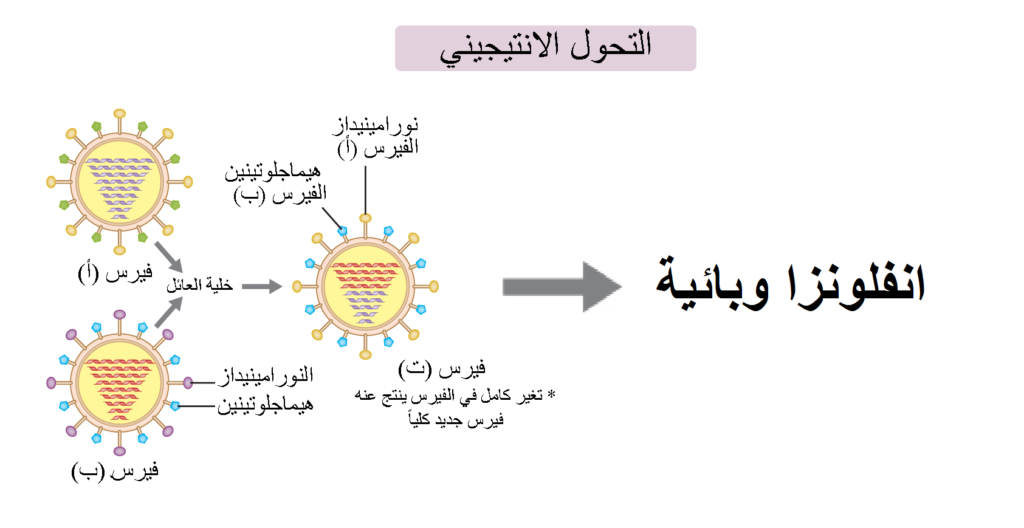
وقد يحدث التغير في المادة الوراثية على نطاق أوسع عن طريق تبادل عدة أجزاء من (vRNPs) بين أكثر من نوع من الإنفلونزا حينما يهاجم فيروسان مختلفان نفس الخلية، فيؤدي إلى تغيّر كبير يتسبب في حدوث الإنفلونزا الوبائية، وتعرف هذه الحالة بـ «التحول الأنتيجيني» (Antigenic Shift) أو «إعادة التشكيل الجيني» (Genetic Reassortment).
ورغم آليات تطور الإنفلونزا ووتيرتها السريعة، يسعى العلماء جاهدين لمواكبة هذا التطور وتطوير لقاح شامل يعتمد في عمله على الأجزاء الثابتة بالبروتينات الشوكية، بالإضافة إلى تطوير عقاقير تعمل على إيقاف دورة تضاعف الفيروس، ومن المحتمل أن ترى إحدى هذه الطرق النور في المستقبل القريب.
المصادر
Shors, Teri. Understanding Viruses. Third edition. Burlington, Massachusetts: Jones & Bartlett Learning, 2017. Print
Principles of Virology, 4th Edition, 1 Vol set by S. Jane Flint, Lynn W. Enquist, Vincent R. Racaniello, Glenn F. Rall, Anna Marie Skalka
Lostroh, P. (2019). Molecular and Cellular Biology of Viruses (1st ed.). Garland Science. https://doi.org/10.1201/9780429021725
3-Krammer, F., Smith, G., Fouchier, R., Peiris, M., Kedzierska, K., Doherty, P. C., Palese, P., Shaw, M. L., Treanor, J., Webster, R. G., & García-Sastre, A. (2018). Influenza. Nature reviews. Disease primers, 4(1), 3. https://doi.org/10.1038/s41572-018-0002-y
Taubenberger JK, Kash JC, Morens DM. The 1918 influenza pandemic: 100 years of questions answered and unanswered. Sci Transl Med. 2019 Jul 24;11(502):eaau5485. doi: 10.1126/scitranslmed.aau5485. PMID: 31341062.
Wei CJ, Crank MC, Shiver J, Graham BS, Mascola JR, Nabel GJ. Next-generation influenza vaccines: opportunities and challenges. Nat Rev Drug Discov. 2020 Apr;19(4):239-252. doi: 10.1038/s41573-019-0056-x. Epub 2020 Feb 14. Erratum in: Nat Rev Drug Discov. 2020 Jun;19(6):427. PMID: 32060419; PMCID: PMC7223957.
Dou, D., Revol, R., Östbye, H., Wang, H., & Daniels, R. (2018). Influenza A Virus Cell Entry, Replication, Virion Assembly and Movement. Frontiers in immunology, 9, 1581. https://doi.org/10.3389/fimmu.2018.01581
Kumar, B., Asha, K., Khanna, M. et al. The emerging influenza virus threat: status and new prospects for its therapy and control. Arch Virol 163, 831–844 (2018). https://doi.org/10.1007/s00705-018-3708-y
Taubenberger JK, Kash JC, Morens DM. The 1918 influenza pandemic: 100 years of questions answered and unanswered. Sci Transl Med. 2019 Jul 24;11(502):eaau5485. doi:10.1126/scitranslmed.aau5485. PMID: 31341062.
Moreira EA, Yamauchi Y, Matthias P. How Influenza Virus Uses Host Cell Pathways during Uncoating. Cells. 2021 Jul 8;10(7):1722. doi: 10.3390/cells10071722. PMID: 34359892; PMCID: PMC8305448.
Avian Flu to Human Influenza David B. Lewis Annual Review of Medicine 2006 57:1, 139-154
Rossman, J. S., & Lamb, R. A. (2011). Influenza virus assembly and budding. Virology, 411(2), 229–236. https://doi.org/10.1016/j.virol.2010.12.003
https://en.wikipedia.org/wiki/Spanish_flu
https://commons.wikimedia.org/wiki/File:InfluenzaNomenclatureDiagram.svg



