
استكشاف العالَم الديناميكي لعلم التخلُّق: عِلم التعبير الجيني خلف تسلسل الحمض النووي
بقلم: معاذ فتح الله
يهتم «عِلم التخلُّق» أو «عِلم ما فوق الجينات» (Epigenetics) بدراسة التغيرات في التعبير الجيني التي لا ترتبط ارتباطًا مباشرًا بالتغيُّرات في تسلسل الحمض النووي. يظل تسلسل الحمض النووي ثابتًا في جميع خلايا الكائن الحي، ويمكن أن يختلف التعبير عن الجينات اعتمادًا على الأنسجة ومرحلة النمو والعوامل البيئية. تلعب التعديلات فوق الجينية دورًا مهمًا في تنظيم التعبير الجيني والحفاظ على الهوية الخلوية، وهي ضرورية للتطور الطبيعي والوظيفة الفسيولوجية.
قدَّم «ديفيد أليس» (David Allis) وزملاؤه مفهوم علم التخلق لأول مرة في عام 1990، حيث وصفوا كيف يمكن لتعديلات فوق جينية أن تنظِّم التعبير الجيني. نما مجال علم التخلق بسرعة كبير منذ ذلك الحين، وتم تحقيق فهم أفضل للآليات الجزيئية للتنظيم فوق الجيني وبرز علم التخلق كمجال رئيسي للبحث في علم الوراثة وعلم الأحياء التنموي وعلم الأمراض.
تتكون الصبغيّات أو «الكروموسومات» (Chromosomes) الحاملة للمادة الوراثية من جزأين هما: الحمض النووي الريبوزي منقوص الأكسجين (DNA) والبروتينات المكونة للصبغيات «الهستونات»(Histones) التي تنظم تشكيله، ويشارك كل منهما بشكل مباشر أو غير مباشر إلى جانب المجموعات (الجزيئات) فوق الجينية في عملية ترجمة الحمض النووي التي ينتج عنها إظهار الصفات الوراثية المختلفة.
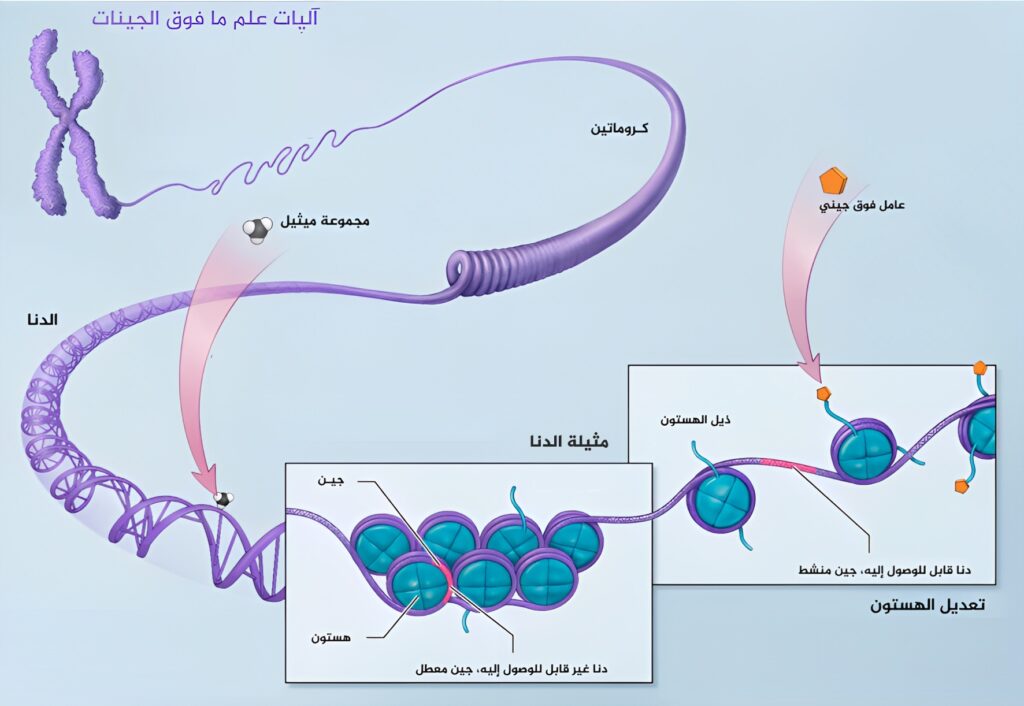
1. آليات التنظيم فوق الجيني (Epigenetic regulation)
يتضمن التنظيم فوق الجيني آليات مختلفة تعدِّل في بنية الحمض النووي أو الهستونات المرتبطة به، ويمكنها تنشيط أو تثبيط التعبير الجيني. تتم العمليات فوق الجينية الرئيسة من خلال ثلاث آليات: تعديل الهستون، و«المَثْيَلَة» (Methylation)، واستخدام «الحمض النووي الريبوزي غير المشفر» (Non-coding RNA).
تُغيِّر التعديلات على بروتينات الهستون من بنيتها، مما يسمح أو يمنع الوصول إلى الحمض النووي الأساسي عن طريق عوامل النسخ والبروتينات التنظيمية الأخرى. تشمل التعديلات عمليات مثل «الأستلة» (Acetylation)، «الفسفرة» (Phosphorylation) و «الوبكنة» (Ubiquitination)؛ وهي إضافة جزيء من بروتينات (Ubiquitin) إلى الهستونات.
أما «المثيلة» فهي إضافة مجموعة ميثيل إلى جزيء الحمض النووي ذاته وبالتحديد عند تتابع نيوكليوتيدات «سيتوزين» (Cytosine) و«جوانين» (Guanine) وهي منطقة يطلق عليها اسم «ثنائي نيوكليوتيدات (CpG)» وتؤدي هذه العملية إلى منع عوامل النسخ من الوصول والارتباط بالحمض النووي وبالتالي تثبيط عملية التعبير الجيني.
من ناحية أخرى، فإن «الأحماض النووية الريبية غير المشفرة»، والتي تتضمن «الرنا الميكروي» (microRNA) و«الرنا الريبي الطويل غير المشفر» (Long non-coding RNA) تُعَدُّ أيضًا منظِّمات جينية مهمة. هنا يرتبط «الرنا الميكروي» بـ «الرنا الرسول» (mRNA) ويقمع ترجمتها، بينما يتفاعل «الرنا الريبي الطويل غير المشفر» مع الإنزيمات المعدلة للكروماتين (Chromatin) وينظم التعبير الجيني على مستوى النسخ.
يؤثر نمط هذه التعديلات في طول «الكروماتين» على بِنيته وبالتالي على عملية التعبير الجيني بالتثبيط أو التنشيط اعتمادًا على موقع وكثافة الجزيئات.
2. دور ما فوق الجينوم في التعبير الجيني والنمو
تلعب التعديلات فوق الجينية دورًا مهمًا في طريقة نمو الكائنات الحية. فأثناء النمو الجنيني، يتم إنشاء أنماط للعلامات فوق الجينية من «مَثْيَلة الحمض النووي» (DNA Methylation) وتعديلات «الهستون» لتحديد مصير الخلية وهويتها عن طريق ما يسمى «التعبير الجيني التفاضلي» (Differential Gene Expression) وهو تغيير في التعبير الجيني حسب نوع الخلية كما هو الاختلاف بين التعبير في خلايا الجلد وخلايا الكبد وغيرها. ويعطي ذلك قدرة للخلايا على التمايز من الخلايا الجذعية داخل الأجنة إلى الأنواع المختلفة من الخلايا ومن ثم نمو أنواع مختلفة من الأنسجة.
تعد التعديلات فوق الجينية ضرورية كذلك لتنظيم التعبير الجيني خلال مراحل مختلفة من الحياة والاستجابة للإشارات البيئية. على سبيل المثال، يمكن أن تحدث «المثيلة» بواسطة إشارات خارجية، مثل الضغط العصبي والتدخين والنظام الغذائي والتلوث البيئي، لتؤثر على التعبير عن الجينات المشاركة في التمثيل الغذائي أو وظائف المناعة.
نتيجة للتباين في التعرض للعوامل المذكورة، لوحظ تباين كبير في ظهور بعض أعراض الشيخوخة في نفس النوع، على الرغم من أن معظم الكائنات الحية لديها منحنيات وفاة مماثلة. كشفت العديد من الدراسات المهتمة بكيفية حدوث الشيخوخة وكيفية تنظيمها بواسطة آليات خلوية وجزيئية أن أحد أهم العوامل المؤثرة هي العوامل فوق الجينية, وهي ما تشارك بشكل مباشر في تنظيم عملية الشيخوخة عن طريق التلاعب بمستويات المَثْيَلة ومن ثم تساهم في إظهار الأمراض المرتبطة بها.
3. التغيرات فوق الجينية والأمراض البشرية
يمكن أن تساهم التغيرات فوق الجينية أيضًا في تطور الأمراض البشرية، مثل السرطان واضطرابات النمو العصبي واضطرابات التمثيل الغذائي. فمن الممكن أن تؤدي تغييرات غير طبيعية في «مثيلة» الحمض النووي إلى تعبير جيني مختل وتثبيط للجينات الكابتة للورم، وبالتبعية تعزيز لنمو الورم الخبيث وانتشاره وتطوره مما يؤدي إلى الإصابة بمرض السرطان.
في اضطرابات النمو العصبي، مثل التوحد والفصام، ارتبطت التغيرات فوق الجينية بتغيير التعبير الجيني وتطور الدماغ غير الطبيعي أثناء التكوين الجنيني لدى المصابين، وفي الاضطرابات الأيضية، مثل السمنة ومرض السكري، قد تؤثر التعديلات فوق الجينية المختلة على التعبير عن الجينات المشاركة في استقلاب الجلوكوز وإشارات الإنسولين سلبًا مؤديةً إلى تراكم الجلوكوز وخلل في تنظيم مستويات الإنسولين.
4. الاتجاهات المستقبلية للعلاجات فوق الجينية
تشمل الاتجاهات المستقبلية في تطوير العلاجات فوق الجينية استخدام تقنيات تحرير ما فوق الجين المستهدف وتطوير العلاجات التوافقية. يتضمن تحرير ما فوق الجين المستهدف تقنيات تحرير الجينوم مثل كريسبر-كاس 9 (CRISPR/Cas9) لتعديل علامات فوق جينية محددة. هذا النهج لديه القدرة على توفير قدر أكبر من الخصوصية والتحكم في التعديلات فوق الجينية ويمكن استخدامه لعلاج مجموعة واسعة من الأمراض.
تميل الاستكشافات نحو تحديد الأساليب التي يمكن أن تستفيد من القدرات المضادة للسرطان للمثبطات فوق الجينية كعوامل مفردة، ويوضح البحث المكثف الذي أجري على مثبطات الجزيئات كأدوات فوق جينية أن البروتينات والإنزيمات المشاركة في العمليات فوق الجينية هي أهداف قابلة للعلاج. في الوقت الحاضر، تمت الموافقة بالفعل من قبل إدارة الأغذية والعقاقير الأمريكية على سبعة مواد دوائية في ثلاث فئات فوق جينية مستهدفة لعلاج الأورام الخبيثة المتنوعة، وتُجرى التجارب السريرية على العديد من المواد الأخرى في الوقت الحالي.
ختامًا، أحدث علم التخلق ثورة في فهمنا للتعبير الجيني وكيف يتم تنظيمه بما يتجاوز مجرد تسلسل الحمض النووي، حيث ثَبَت أن آليات التنظيم فوق الجيني تلعب أدوارًا حاسمة في التعبير الجيني والتطور.
علاوة على ذلك، تورّطت التغيرات فوق الجينية في مجموعة واسعة من الأمراض البشرية، مثل السرطان، واضطرابات النمو العصبي، واضطرابات التمثيل الغذائي. ومع تطور العلاجات فوق الجينية فهناك أمل كبير للعلاجات الجديدة التي تستهدف التعديلات فوق الجينية لمنع هذه الأمراض أو علاجها.
وعلى الرغم من أنه لا يزال هناك الكثير للتعرف عليه عن العالم الديناميكي لعلم التخلق، فمن الواضح أن هذا المجال يحمل إمكانية هائلة للتقدم في فهمنا لصحة الإنسان ومرضه. على هذا النحو، فإن استمرار البحث والتنمية في علم التخلق سيمهد بلا شك الطريق لنهج جديدة ومبتكرة لتحسين صحة الإنسان ورفاهيته.
المصادر:
Lacal, I., & Ventura, R. (2018). Epigenetic Inheritance: Concepts, Mechanisms and Perspectives. Frontiers in Molecular Neuroscience, 11.
Nepali, K., Liou, JP. Recent developments in epigenetic cancer therapeutics: clinical advancement and emerging trends. J Biomed Sci 28, 27 (2021).
Moosavi A, Motevalizadeh Ardekani A. Role of Epigenetics in Biology and Human Diseases. Iran Biomed J. 2016 Nov; 20(5):246-58. doi: 10.22045/ibj.2016.01. Epub 2016 Jul 5. PMID: 27377127; PMCID: PMC5075137.



