فيزياء السرطان: نهج واعد نحو الاستهداف الانتقائي
طبقًا لمنظمة الصحة العالمية، فالسرطان ثاني الأمراض فتكًا حول العالم بمعدل عشرة ملايين وفاة سنويًا، وهذا العدد المتزايد يعود للإصابة بالنوع الخبيث من السرطان، والذي يُعرَف بـ«السرطان النُقيلي» (Metastasis)؛ هذا النوع عبارة عن هجرة بعض الخلايا السرطانية من موقع الإصابة الأصلي لأجزاء متفرقة من الجسم عبر انبثاثها للدورة الدموية أو الليمفاوية واستقرارها بأعضاء مختلفة، مما يتسبب في تكوين بؤر خبيثة منتشرة على طول جسد المريض، وهذا التفشي هو ما جعل العلاجات التقليدية لا تزال عاجزة عن استهدافه دون إصابة الأنسجة السليمة المحيطة بأضرار مدمرة.
جذور المشكلة
منذ اكتشاف السرطان وحتى الآن، لدينا عدة خيارات غير جراحية تتمثل في العلاج الكيميائي والإشعاعي والهرموني والمناعي، حيث إن لكل منها ميزة طبية خاصة. ولكن العقبة تكمن في آثارها الجانبية الناتجة عن ضعف قدراتها على «الاستهداف الانتقائي» (Selective Targeting) للورم؛ وهو إصابة الخلايا الخبيثة دون إصابة الخلايا الطبيعية بضرر.
يمكننا ملاحظة الرابط بين تلك التقنيات العلاجية المختلفة، وهو اعتمادها على مهاجمة السرطان من خصائص “تتشارك” فيها مع الخلايا الطبيعة، فمثلًا: ينقسم السرطان بمعدل سريع نتيجة خلل جيني. ومن ثَمَّ، عند تصميم علاج ما يستغل تلك الصفة غير المميزة، فإن ذلك العلاج لن يفرِّق في هجومه بين الورم وبين الخلايا السليمة التي تنقسم سريعًا بشكل طبيعي (مثل خلايا نخاع العظم أو الخلايا المعوية)، وهذا الضرر الجانبي غير قابل للتجاوز.
طوال العقود السابقة، ظل استخدام تلك التقنيات النهج السائد للوسط العلمي، حتى استطعنا دراسة بعض الخصائص الفيزيائية للخلايا، مثل الخصائص الميكانيكية والحرارية والكهربية والضوئية، وبيان الاختلافات بين التكوين الطبيعي وبين الانحرافات البنيوية نتيجة الشذوذ الخلوي مثل «عملية التسرطن» (Cancerogenesis)، مما فتح طريقًا جديدًا لمواجهة السرطان والأمراض الخلوية الأخرى. 1,2
الفيزياء تكشف التباين
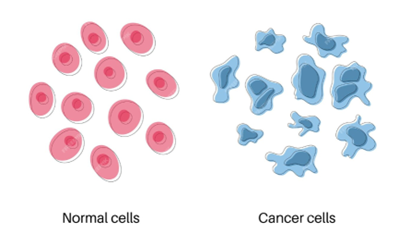
أثبتت الأبحاث من مجالات متعددة أن السرطان يتباين في كل الظواهر الفيزيائية على المستويين الخلوي والنسيجي كنتيجة طبيعية للطفرات الجينية المتعددة، ويظهر ذلك من فحص الاضطرابات البنائية والسلوكية للسرطان، حيث إنه عادة ما يُشخَّص السرطان بناءً على «مظهر الخلية» (Cell Morphology)، والتي تكون ذات حجم أكبر، وغشاء خلوي متعرج وغير منتظم، ونواة مشوهة تحتل الجزء الأكبر من السيتوبلازم كما يظهر بالشكل (1).
كل ما سبق يمثِّل الصفات الفيزيائية المميزة لبنية الخلية السرطانية، فعلى سبيل المثال: نجد أنه من الناحية الميكانيكية، غالبًا ما تُظهِر الخلايا السرطانية الخبيثة انخفاضًا في «الصلابة» (Stiffness)؛ مما يجعلها لينة وأكثر قابلية للتشوه، ويُعتقَد أن هذا هو السبب الفيزيائي وراء قدرة الورم على الهجرة من موقع لآخر.6–1
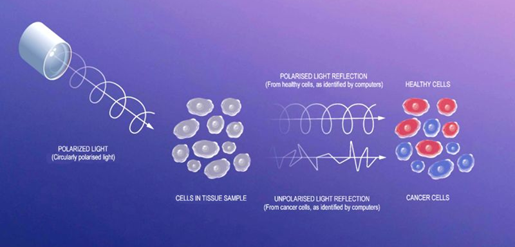
في الآونة الأخيرة، تمكنَّا من استخدام الخصائص غير المرئية للضوء لتشخيص السرطان في وقت أقصر من المعتاد عبر استغلال تلك التشوهات المورفولوجية لخلايا السرطان، والتي تظهر بوضوح من خلال تعريض العينة لنوع من الضوء المستقطَب، حيث إن موجات الضوء تلك تتذبذب مجالاتها الكهربائية في اتجاه واحد معين، بدلًا من التذبذب في جميع الاتجاهات. لا تستطيع أدمغتنا اكتشاف هذه الخاصية، لذا فهذا النوع من الضوء غير مرئي بالنسبة لنا.
أثبتت الأبحاث إمكانية استخدام «التذبذب الدائري من الضوء المستقطَب» (Circular Polarized Light) الذي يهتز في مسار دائري على طول اتجاه الانتشار -كما هو موضح بالشكل (2)- للتمييز بين الأنسجة السليمة والسرطانية. حيث إنه عند تعرُّض «الخزعة» (Biopsy) لهذه الموجات المستقطبة، فإن أنوية الخلايا السليمة تُشتت الضوء بنفس نمط اهتزازه الدائري الأصلي دون انحراف. على عكس الخلايا السرطانية التي تكون نواتها ذات بنية مشوَّهة وحجم أكبر من الطبيعي، وعليه فإن الموجات الصادرة منها لها نمط فوضوي غير منتظم. وباستخدام خوارزميات الذكاء الاصطناعي، يمكن أتمتة عملية تشخيص السرطان استنادًا لتلك الخصائص الفيزيائية -الضوئية- المميزة.7
السلوك المُتفرِّد للسرطان
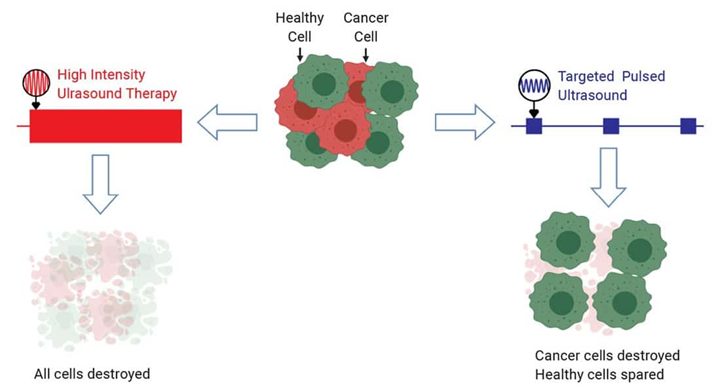
عند دراسة السلوك الحراري للسرطان، نجد أنه ذو حساسية أعلى تجاه التغيرات الحرارية، ربما يعود ذلك للنشاط الأيضي المفرط للخلية السرطانية، والذي يُعَد سمة أساسية للسرطان، خصوصًا المراحل المتقدمة منه، ولذا كانت التقنيات العلاجية المعتمدة على «فرط الحرارة» (Hyperthermia) ناجحة في الاستئصال الموضعي. على سبيل المثال، العلاج بالموجات الصوتية التقليدية -ذات الشدة العالية- يؤدي للتسخين المتجانس للمنطقة المعرَّضة له، وهذا الأثر غير مناسب لكل حالات السرطان، بالإضافة لإصابة الخلايا المحيطة بالورم بأضرار قاتلة كما يتضح من الجزء الأيسر للشكل (3)، ولذلك لا يمكن الاعتماد على هذا المفهوم لتعدد آثاره الجانبية.
ركزت الأبحاث حديثًا على التقنيات الفيزيائية الموجهة، إذ يتغير نمط سلوك الخلية السرطانية بسبب التشوهات البنائية التي تصيبها؛ فلكل نظام طبيعي تردد اهتزاز فريد يمثل حالة الاستقرار المُثلَى، وهو ما يُعرَف بـ«تردد الرنين» (Resonance Frequency). وعند حدوث أي تغير كيميائي او هيكلي للنظام، فإن تردده يتغير ويصبح له تردد رنين جديد، وهذا ما تستغله تقنية العلاج «بالموجات فوق الصوتية منخفضة الكثافة» (Low-Intensity Pulsed Ultrasound)، حيث لأغشية الخلايا السرطانية استجابات اهتزازية عند ترددات معينة -حوالي 500 كيلو هيرتز- ولذا عند تعريضها لنبضة لمدة 2-40 مللي ثانية عند نفس التردد، تتدمر الأغشية السرطانية بشكل انتقائي دون أثر جانبي على الخلايا الطبيعية، كما يظهر في الجزء الأيمن من الشكل (3). هذا التقنية تندرج تحت مفهوم واسع يُسمَّى «تفتيت الورم» (Oncotripsy)، وهو إصابة السرطان بناء على خصائص رنينه الفريدة، وهذا ما أثبتت فعاليته النماذج النظرية الحاسوبية، إلى أن تخرج الدراسات الإكلينيكية للنور.1,4,8,9
مستقبل الفيزياء الحيوية
يعود الفضل للتكنولوجيا الحديثة في الكشف عن الخصائص الفيزيائية للنظم الحيوية بمستويات تعقيدها المختلفة -الخلوي والنسيجي والعضوي- وهذا ما وفر للباحثين كميات هائلة من البيانات التي تنتظر النماذج الملائمة لتفسيرها واستغلالها. أصبح النهج الجديد في فهم الخصائص الحيوية مؤخرًا (مثل: التكاثر، التكيف، التواصل، وغيرها) من خلال دراسة التغيرات الفيزيائية البنيوية والسلوكية.
ولم يتوقف الأمر عند ذلك الحد، بل من خلال مقارنة تلك التغيرات بين حالات الصحة والمرض للنظام، يمكننا الكشف عن الأنماط المورفولوجية المميزة لكل مرض، وهذا ما يؤدي لتطوير علاجات أكثر كفاءة وقابلية للاستهداف بناءً على الصفات الفيزيائية المميزة. لذلك، كلما استطعنا فهم العلاقة بين فيزياء الأنظمة الحيوية وبين السلوكيات المعقدة للحياة، اقتربنا أكثر من فهم الحياة كظاهرة فيزيائية بشكل أعمق، بالإضافة لتوفير بيئة طبية أفضل.
المصادر
1. Mierke, C. T. Physics of Cancer, Volume 5 (Second Edition). Physics of Cancer, Volume 5 (Second Edition) (IOP Publishing, 2023). doi:10.1088/978-0-7503-6274-0.
2. White, F. M., Gatenby, R. A. & Fischbach, C. The physics of cancer. Cancer Res 79, 2107–2110 (2019).
3. Liu, S. et al. Mechanotherapy in oncology: Targeting nuclear mechanics and mechanotransduction. Advanced Drug Delivery Reviews vol. 194 Preprint at https://doi.org/10.1016/j.addr.2023.114722 (2023).
4. Bergman, E. et al. Cell stiffness predicts cancer cell sensitivity to ultrasound as a selective superficial cancer therapy. Bioeng Transl Med 6, (2021).
5. Iyer, S., Gaikwad, R. M., Subba-Rao, V., Woodworth, C. D. & Sokolov, I. Atomic force microscopy detects differences in the surface brush of normal and cancerous cells. Nat Nanotechnol 4, 389–393 (2009).
6. Korgaonkar, N. & Yadav, K. S. Understanding the biology and advent of physics of cancer with perspicacity in current treatment therapy. Life Sciences vol. 239 Preprint at https://doi.org/10.1016/j.lfs.2019.117060 (2019).
7. Nishizawa, N., Al-Qadi, B. & Kuchimaru, T. Angular optimization for cancer identification with circularly polarized light. J Biophotonics 14, (2021).
8. Heyden, S. & Ortiz, M. Oncotripsy: Targeting cancer cells selectively via resonant harmonic excitation. J Mech Phys Solids 92, 164–175 (2016).
9. David R. Mittelstein, Jian Ye, Erika F. Schibber, Ankita Roychoudhury, Leyre Troyas Martinez, M. Houman Fekrazad, Michael Ortiz, Peter P. Lee, Mikhail G. Shapiro, Morteza Gharib; Selective ablation of cancer cells with low intensity pulsed ultrasound. Appl. Phys. Lett. 6 January 2020; 116 (1): 013701.



